2023年10月26日,百吉生物在CGT实体瘤范畴又一重磅产物BST02的I/II期临床实验申请取得美国FDA核准,用在医治所有类型的肝癌,是全球首款进入临床阶段针对肝癌的TIL细胞医治药品。
TIL疗法是指从肿瘤组织平分离天然浸润淋巴细胞,经由过程体外扩增和功能优化后,从头回输到患者体内。因为TIL具有多种TCR克隆性、选择性肿瘤归巢能力和较低的非肿瘤靶向毒性,TIL疗法在实体瘤的细胞免疫疗法范畴具有极年夜的优势。
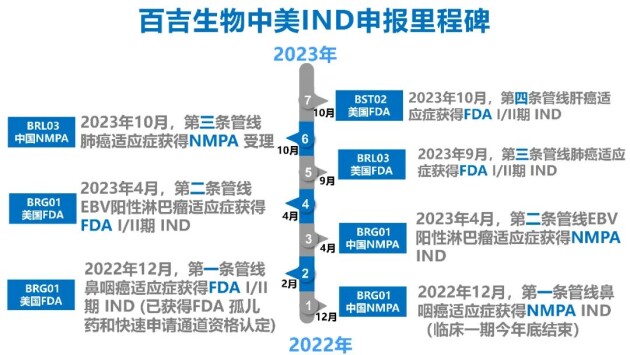
作为百吉生物第四条全球初创产物管线,此次BST02(TIL疗法)临床实验申请的成功获批,是百吉生物依托独有的高效全球一体化研发转江南体育化系统实现的又一重年夜里程碑。百吉生物在曩昔10个月内持续4条初创管线前后取得中美两国IND核准,标记着百吉生物已成为同时笼盖CAR-T、TCR-T、TIL三年夜T细胞医治范畴的国际领先原研药企。
从CAR-T、TCR-T再到TIL,它们代表了操纵肿瘤特异性T细胞医治实体瘤的新冲破。虽然细胞疗法整体研发线路一致,但是,分歧细胞疗法也有分歧的手艺线路,乃至同种细胞的分歧产物也会利用分歧的研产生产手艺。今朝,百吉生物搭建了包罗IDENTIFIER®在内的多方面手艺平台和数据库,为抗原、抗体和TCR发现判定,和结构分歧细分医治产物供给坚实的支持。厚积薄发,行稳致远,百吉生物将继续对峙始终办事在患者未被知足临床需求,开辟更多全球初创、极具价值的免疫医治药品,造福全球患者。
关在BST02
原发性肝癌(primary liver cancer,PLC)简称肝癌,是全球规模内常见的消化系统恶性肿瘤,包罗肝细胞癌(HCC)和肝内胆管癌(ICC)等。按照 GLOBOCAN 2020发布的新数据,全球肝癌的年新病发例数到达90.6万人,居在恶性肿瘤第7位,灭亡83.0万人,居在恶性肿瘤的第2位。原发性肝癌在我国特别多发,是第4位的常见恶性肿瘤和第2位的肿瘤致死病因。我国生齿仅占全球的18.6%,可是肝癌年新病发例到达41.0万人,灭亡39.1万人,别离到达全球的45.3%和47.1%,肝癌严重地要挟我国人平易近的生命和健康。
百吉生物研制的BST02打针液是一款从患者本身肿瘤浸润淋巴细胞中扩增所获得的T细胞医治产物,用在医治肝癌(包罗肝细胞癌和胆管癌),属在过继性免疫细胞医治手艺。
其根基道理是,从患者本身的肿瘤组织中收集并富集具有特异性辨认肿瘤细胞抗原能力的淋巴细胞,在体外经由过程细胞因子引诱快速增殖并保持其干性,以最年夜限度扩增具有抗肿瘤功能的T细胞,再回输到患者体内,终究实现对肿瘤起杀伤结果的一种细胞医治药物。传统TIL药物在利用时存在一些限制,好比要求药品出产地与临床中间距离近,临床利用中需要高剂量白介素-2联用,可能会带来必然的平安性隐患等。
百吉生物的BST02是冻存产物,冲破了距离的限制,且不需要高剂量白介素-2陪伴用药,其平安性和有用性已在摸索性临床中获得初步验证。
关在百吉生物

百吉生物是一家专注细胞与基因医治具有国际竞争力的立异药公司,首要致力在免疫细胞医治范畴的研究和立异,力争为肿瘤患者供给最好的医治方案。
百吉生物会聚新加坡、中国、德国、澳国、法国、美国三地六国顶尖科研人材,博士研发团队中卒业在全球排名前50年夜学的比例达80%,广州、新加坡别离具有华南地域最年夜的和新加坡最年夜的私立GMP细胞出产与研发基地,安身亚洲,面向全球,今朝已结构产物市场范围超500亿美金。
百吉生物在医治鼻咽癌、多种消化道类肿瘤、肝癌、肺癌、EBV阳性血液系统疾病等多种实体瘤和血液瘤范畴具有全球初创/同类最好产物,其全球独家初创的BRG01 打针液新药临床实验(IND)正式取得国度药品监视治理局药品审评中间的临床实验默示许可和美国食物药品监视治理局(FDA)Ⅰ/Ⅱ期临床实验许可。针对鼻咽癌免疫细胞医治药品BRG01被美国FDA授与“孤儿药资历认定”(ODD)和快速通道资历(FTD)。另外,BRL03也取得美国FDAⅠ/Ⅱ期临床实验许可和NMPA IND 受理。百吉生物也是业内领先的产物管线同时笼盖 CART、TCRT、TIL等多种前沿免疫细胞医治范畴的生物科技公司。
百吉生物在新加坡、中国广州别离设有总部,与新加坡科技研究局(A*STAR)、慕尼黑赫姆霍兹中间(Helmholtz Zentrum München)、德国汉诺威医学院、中山年夜学从属肿瘤防治中间、复旦年夜学从属肿瘤病院(排名不分前后)和十多家三甲病院成立了慎密的研究合作关系,多管线产物在新加坡、Australia、中国等国度展开临床实验。
百吉生物在新加坡和广州具有成熟的手艺研发和转化平台,手艺立异和堆集能力笼盖成药性研究、临床前研究、临床研究和出产转化等药品开辟全周期,在国表里别离具有双GMP出产与新药研发基地,实现了集研发、出产、发卖在一体的全财产链结构。

 责任编纂:Linda
责任编纂:Linda